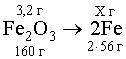358
476
всего разделов:
активных пользователей:
30 мартра 2005
Форумы снова функционируют.
21 декабря 2004
Видимо в связи с обнаруженными дырами в phpBB, форум был взломан, а через него взломано и всё остальное содержимое ceemat.ru. Всё кроме форума восстановлено, ведется дискуссия по поводу его сохранения.
Приносим извинения за неудобства.
29 сентября 2004
Форум обновился до версии 2.0.10
15 мая 2004
Новый раздел: "Программирование"
16 апреля 2004 года
Задачи Ярославского турнира математических боев — 124 задачи с решениями.
29 марта 2004
Таллинская викторина: занимательные вопросы и задачи для увлеченных химией.
10 класс (5)
Установите формулу кристаллогидрата двойной соли сульфата железа и аммония, если при растворении 19,28 г ее в воде и добавлении крепкой щелочи выделяется 896 мл газа и бурый осадок, который после прокаливания весит 3,2 г. |
1. После действия крепкой щелочи выделяется аммиак и бурый осадок гидроксида железа, следовательно взята соль Fe (III). 2. 2Fe(OH)3 → Fe2O3 + 3H2O (1) 3. Рассчитаем количество железа в кристаллогидрате:
X = 1 · 56 · 3,2/160 = 2,24 г n(Fe) = 2,24/56 = 0,04 моль 4. n(NH3) = 0,896/22,4 = 0,04 моль 5. Соотношение солей 1 : 1 (следует из количеств аммиака и железа), следовательно в состав двойной соли входит (NH4)2SO4 и Fe2(SO4)3. 6. Масса сульфатов железа и аммония: n((NH4)2SO4)= n(Fe2(SO4)3) = 0,02 моль (0,04/2) m = 132 · 0,02 + 400 · 0,02 = 10,64 г М((NH4)2SO4) = 132 г/моль; М(Fe2(SO4)3) = 400 г/моль 7. Масса воды: 19,28 г – 10,64 г = 8,64 г n(Н2O) = 0,48 моль 8. Соотношение молей (NH4)2SO4 : Fe2(SO4)3 : Н2O = 0,02 : 0,02 : 0,48 или 1 : 1 : 24. 9. Формула кристаллической двойной соли: (NH4)2SO4 · 2Fe2(SO4)3 · 24Н2O или NH4Fe(SO4)2 · 12Н2O |
18 Марта 2004 21:23 Раздел каталога :: Ссылка на задачу
|