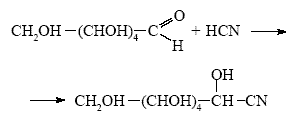358
476
всего разделов:
активных пользователей:
30 мартра 2005
Форумы снова функционируют.
21 декабря 2004
Видимо в связи с обнаруженными дырами в phpBB, форум был взломан, а через него взломано и всё остальное содержимое ceemat.ru. Всё кроме форума восстановлено, ведется дискуссия по поводу его сохранения.
Приносим извинения за неудобства.
29 сентября 2004
Форум обновился до версии 2.0.10
15 мая 2004
Новый раздел: "Программирование"
16 апреля 2004 года
Задачи Ярославского турнира математических боев — 124 задачи с решениями.
29 марта 2004
Таллинская викторина: занимательные вопросы и задачи для увлеченных химией.
11 класс (8)
В черновиках Агаты Кристи описан следующий эпизод: "Некий коммерсант, решив покончить со своими конкурентами, пригласил их в гости и приготовил ядовитую смесь, прокалив сухой остаток бычьей крови с углем. Один из гостей любил сухое вино, а другой предпочитал сладкое. Коммерсант незаметно подмешал яд в вино и, провозгласив тост, стал наблюдать за своими гостями. Допив свой бокал, первый гость схватился за горло, зашатался и упал; его губы посинели, и через несколько минут он скончался. Второй гость почувствовал лишь легкое недомогание и поспешил покинуть "гостеприимный дом", захватив с собой рюмку с остатками вина, чтобы провести его химический анализ. В лаборатории слили вино и выделили 0,500 г вещества, которое обработали соляной кислотой и получили 89,6 мл газа (н.у.), причем в рюмке осталось 0,140 г нерастворившегося черно-серого вещества. При сжигании газа образовалось 44,8 мл (н.у.) углекислого газа и 0,108 г воды."
|
1. При прокаливании сухого остатка крови с углем происходит пиролиз всех органических веществ, содержащихся в крови, выделяются пары воды, а содержащийся в крови азот переходит в анион CN-, который образует калиевые и натриевые соли (натрий содержится в плазме крови, а калий - в древесном угле). Экстракция этого плава спиртом позволяет получить спиртовой раствор KCN и NaCN. В сухом вине содержатся этиловый спирт, вода, пахучие вещества, винные кислоты и их соли. Поэтому тот из гостей, который предпочитал сухое вино, с первыми глотками получил смертельную дозу цианида и сразу умер. Известно, что моносахариды присоединяют HCN в нейтральной среде. Циановодород образуется при действии на цианиды калия и натрия кислот, содержащихся в вине. В сладком вине HCN прореагировал с глюкозой с образованием циангидрина, который не является ядовитым:
Поэтому этот гость остался в живых. 2. Кроме KCN и NaCN в ядовитой смеси находились по крайней мере еще два вещества. Нерастворимое в соляной кислоте вещество, по всей вероятности, представляет собой углерод, а растворимое вещество — карбид. Определим количества С и Н в продуктах сгорания выделившегося газа: n(C) = 0,0448/22,4 = 0,002; n(H) = 0,108 · 2/18 = 0,012; n(H) : n(C) = 6 : 1. Максимально возможное для всех углеводородов и кислородсодержащих веществ отношение n(H) : n(C) = 4. Следовательно, речь идет о смеси газов, один из которых — водород. Пусть газ состоит из СaНb и Н2. По данным анализа можно составить систему уравнений: n(СaНb) + n(Н2) = 0,0896/22,4 = 0,004, n(СaНb)b + n(Н2) · 2 = 0,012, n(СaНb)a = 0,002. Решение этой системы дает b = 2a + 2. Таким образом, смесь газов содержит только предельные углеводороды и водород: при a = 1 n(СН4) = 0,002 и n(Н2) = 0,002; при а = 2 n(С2Н6) = 0,001 и n(Н2) = 0,003; при а = 3 n(С3Н8) = 0,00067 и n(Н2) = 0,00333. Далее примем, что выделяющийся газ содержит только метан и водород в мольном соотношении 1 : 1, тогда уравнение разложения карбида соляной кислотой в общем виде выглядит следующим образом: MxCy + xzHCl = xMClz + yCH4 + yH2 По условию можно составить систему уравнений: (0,5 - 0,14)/(xM + 12y) = 0,0896/(44,8y), xz = 6y. Отсюда М = 28z. При z = 2, М = 56, что соответствует молярной массе железа. В карбиде отношение количеств железа и углерода равно 3 (так как 2x = 6y). Тогда уравнение реакции имеет вид Fe3C + 6HCl = 3FeCl2 + CH4 + H2 Следовательно, при приготовлении ядовитой смеси произошла следующая реакция: K4[Fe(CN)6] = 4KCN + Fe3C + N2 + C |
22 Февраля 2004 21:30 Раздел каталога :: Ссылка на задачу
|