358
476
всего разделов:
активных пользователей:
30 мартра 2005
Форумы снова функционируют.
21 декабря 2004
Видимо в связи с обнаруженными дырами в phpBB, форум был взломан, а через него взломано и всё остальное содержимое ceemat.ru. Всё кроме форума восстановлено, ведется дискуссия по поводу его сохранения.
Приносим извинения за неудобства.
29 сентября 2004
Форум обновился до версии 2.0.10
15 мая 2004
Новый раздел: "Программирование"
16 апреля 2004 года
Задачи Ярославского турнира математических боев — 124 задачи с решениями.
29 марта 2004
Таллинская викторина: занимательные вопросы и задачи для увлеченных химией.
10 класс (10)
Прямая перегонка нефти дает относительно небольшое количество бензина, причем качество этих бензинов, равно как и бензинов, получаемых при крекинге, бывает недостаточно хорошим. Для улучшения качества бензинов как моторного топлива для двигателей внутреннего сгорания используются специальные добавки. В лабораторию одного из исследовательских институтов было представлено на исследование два образца бензинов улучшенного качества, выпущенных зарубежными фирмами. При перегонке образцов из кубовых остатков были выделены твердые окрашенные вещества X и Y, в спектрах ПМР которых обнаруживается один сигнал протонов. При элементном анализе соединений X и Y сожжением в кислороде получены следующие данные:
(в последней строчке приведены отношения масс несгораемого остатка при сожжении к массе анализируемой навески, которые меняются в указанных интервалах в зависимости от условий сожжения). Вещества X и Y не присоединяют водород при 20-80 °С, но при 300 °C под давлением X и Y образуют один и тот же углеводород A, содержащий 85,7% углерода. В обоих случаях масса используемого платинового катализатора возрастает. Увеличение массы для X составляет 30%, а для Y — 27% по отношению к массе навески, взятой для гидрирования. Обработка осадка катализатора разбавленной соляной кислотой в случаях X и Y приводит к количественной регенерации платины. Полученные при очистке платины растворы X1 и Y1 слабо окрашены. При добавлении этих растворов к избытку раствора щелочи выпадают белые быстро темнеющие осадки. При действии избытка хлора на X и Y образуется одна и та же жидкость B, содержащая 24,74% C, 2,06% H, 73,20% Cl, а также твердые окрашенные соединения X2 и Y2.
| ||||||||||||
Ответ: X — (C5H5)2Fe, Y — C5H5Mn(CO)3, A — C5H10, B — C5H5Cl5, X1 — FeCl2, Y1 — MnCl2, X2 — FeCl3, Y2 — MnCl2. Вещества Х и Y содержат C, H и металл, и, вероятно, представляют собой металлоорганические соединения. При каталитическом гидрировании происходит выделение металлов в свободном состоянии. Величины прироста массы катализатора соответствуют процентному содержанию металла. Суммарное количество этих элементов в соединении Х равно 64,5 + 5,4 + 30 = 99,9%, и можно предположить, что Х имеет формулу CxHyM(1)z. Атомное соотношение C : H в Х равно При сожжении вещества такого состава в кислороде наряду с CO2 и H2O будут получаться оксиды железа (в зависимости от условий — от FeO до Fe2O3). Приведенные соотношения масс несгораемого остатка m/m0 соответствуют образованию этих оксидов: (C5H5)2Fe + (12,5 + 0,5y)O2 → 10CO2 + 5H2O + FeOy (y = 1-1,5). Гидрирование Х протекает по уравнению (C5H5)2Fe + 5H2 → 2C5H10 + Fe при этом образуются циклопентан C5H10 (85,7% C) и металлическое железо, дальнейшие превращения которого, описанные в условии, протекают по уравнениям Fe + 2HCl = H2 + FeCl2
FeCl2 + 2KOH = 2KCl + Fe(OH)2 4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3 Fe(OH)2 — белый осадок, темнеющий на воздухе. При действии хлора происходит разрушение Х по уравнению (C5H5)2Fe + 6,5Cl2 → 2C5H5Cl5 + FeCl3 В результате этой реакции образуется Для соединения Y сумма процентного содержания C, H, M(2) равна 47,1 + 2,45 + 27 = 76,55. Можно предположить, что недостающая до 100% часть приходится на кислород. В этом случае атомное соотношение При хлорировании Y образуется то же соединение B, что и при хлорировании X. Это означает, что в состав Y входит группировка C5H5, а Y описывается формулой C5H5Mn(CO)3. Описанные в условиях превращения соответствуют уравнениям: C5H5Mn(CO)3 + (4,75 + 0,5y)O2 → 5CO2 + 2,5H2O + MnOy (y = 1-2)
C5H5Mn(CO)3 + 5,5H2 → C5H10 + Mn + 3H2O
C5H5Mn(CO)3 + 6,5Cl2 → C5H5Cl5 + MnCl2 + 3COCl2 (при хлорировании Y образуются MnCl2 и тот же Mn + 2HCl → H2 + MnCl2
MnCl2 + 2KOH → Mn(OH)2 + 2KCl 2Mn(OH)2 + O2 → 2MnO2 + 2H2O (упрощенно);
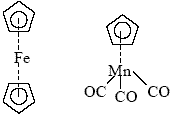
Нетоксичные железоорганические соединения — ферроцен (C5H5)2Fe и его производные, а также марганецорганические соединения — цимантрен C5H5Mn(CO)3 и его производные — могут быть использованы как хорошие антидетонаторы для моторного топлива вместо чрезвычайно ядовитых свинецорганических соединений и, в частности, вместо тетраэтилсвинца (C2H5)4Pb (этиловой жидкости), вызывающего сильнейшие загрязнения окружающей среды. Оба металлорганических соединения — ферроцен и цимантрен — принадлежат к классу Ι-комплексов, построенных за счет электронного взаимодействия незаполненных орбиталей атомов переходных металлов с электронами ароматических циклопентадиениланионов (и электронами CO). Ферроцен имеет пространственную структуру сэндвича (бутерброда), а цимантрен по структуре похож на фортепианную табуретку:
| ||||||||||||
15 Февраля 2004 17:33 Раздел каталога :: Ссылка на задачу
| ||||||||||||