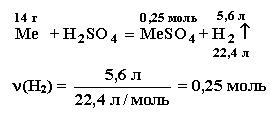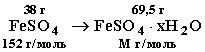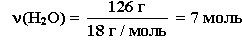358
476
всего разделов:
активных пользователей:
30 мартра 2005
Форумы снова функционируют.
21 декабря 2004
Видимо в связи с обнаруженными дырами в phpBB, форум был взломан, а через него взломано и всё остальное содержимое ceemat.ru. Всё кроме форума восстановлено, ведется дискуссия по поводу его сохранения.
Приносим извинения за неудобства.
29 сентября 2004
Форум обновился до версии 2.0.10
15 мая 2004
Новый раздел: "Программирование"
16 апреля 2004 года
Задачи Ярославского турнира математических боев — 124 задачи с решениями.
29 марта 2004
Таллинская викторина: занимательные вопросы и задачи для увлеченных химией.
9 класс (5)
Распределение баллов по задачам:
| № задачи | 1 | 2 | 3 | 4 | 5 |
| Максимальный балл | 8 | 11 | 12 | 11 | 8 |
Определите формулу кристаллогидрата, если при растворении 14 г неизвестного металла в разбавленной серной кислоте выделилось 5,6 л водорода и образуется соль MeSO4, из которой можно получить 69,5 г кристаллогидрата. Его можно использовать в производстве красок и для пропитки древесины для предотвращения ее гниения. |
Записываем уравнение реакции между металлом и кислотой в общем виде:
По уравнению ν(Ме) = ν(MeSO4) = 0,25 моль Относительная атомная масса металла может быть найдена 2 способами: Ar = 22,4 · 14/5,6 = 56 или Ar = 14/0,25 = 56, следовательно, это железо. Формула соли FeSO4, а кристаллогидрата — FeSO4 · хН2О. Рассчитываем массу безводной соли:
М(FeSO4 · хН2О) = 278 г/моль Масса воды в кристаллогидрате: m(Н2О) = 278 г - 152 г = 126 г Находим количество вещества воды:
следовательно, формула кристаллогидрата FeSO4 · 7Н2О. |
Авторы — Т.П.Шулятьева, Ю.С.Чумаков Разбалловка решения задачи:
Итого: 11 баллов |
30 Января 2004 16:53 Раздел каталога :: Ссылка на задачу
|