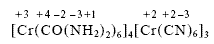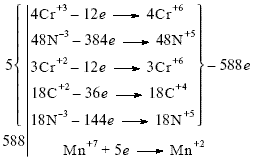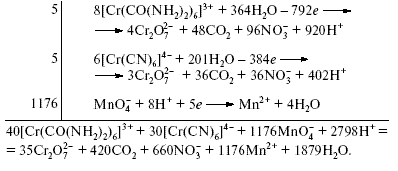358
476
всего разделов:
активных пользователей:
30 мартра 2005
Форумы снова функционируют.
21 декабря 2004
Видимо в связи с обнаруженными дырами в phpBB, форум был взломан, а через него взломано и всё остальное содержимое ceemat.ru. Всё кроме форума восстановлено, ведется дискуссия по поводу его сохранения.
Приносим извинения за неудобства.
29 сентября 2004
Форум обновился до версии 2.0.10
15 мая 2004
Новый раздел: "Программирование"
16 апреля 2004 года
Задачи Ярославского турнира математических боев — 124 задачи с решениями.
29 марта 2004
Таллинская викторина: занимательные вопросы и задачи для увлеченных химией.
11 класс (10)
Авторы задач и решений:
В.В. Еремин, Г.А. Середа, С.С. Чуранов, Д.О. Чаркин
Один американский профессор решил проверить своих коллег на умение уравнивать окислительно-восстановительные реакции и предложил им “химического монстра”: уравнение реакции окисления комплекса
|
1. Заряд катиона равен + 3, аниона - 4. Мочевина (NH2)2CO электронейтральна, ион CN- имеет заряд -1, поэтому в катионе хром имеет степень окисления + 3, а в анионе + 2. Остальные степени окисления — обычные:
2. Схема реакции:
[Cr(CO(NH2)2)6]4[Cr(CN)6]3 + KMnO4 + H2SO4 → 3. а) Электронный баланс:
Полученные коэффициенты 5 и 588 нужно еще умножить на 2, чтобы получить в левой части четное число атомов хрома, так как в правой части есть дихромат калия K2Cr2O7 с двумя атомами хрома. Окончательное уравнение:
10[Cr(CO(NH2)2)6]4[Cr(CN)6]3 + 1176KMnO4 + 1399H2SO4 = б) Электронно-ионный баланс:
|
5 Января 2004 16:51 Раздел каталога :: Ссылка на задачу
|