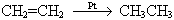358
476
всего разделов:
активных пользователей:
30 мартра 2005
Форумы снова функционируют.
21 декабря 2004
Видимо в связи с обнаруженными дырами в phpBB, форум был взломан, а через него взломано и всё остальное содержимое ceemat.ru. Всё кроме форума восстановлено, ведется дискуссия по поводу его сохранения.
Приносим извинения за неудобства.
29 сентября 2004
Форум обновился до версии 2.0.10
15 мая 2004
Новый раздел: "Программирование"
16 апреля 2004 года
Задачи Ярославского турнира математических боев — 124 задачи с решениями.
29 марта 2004
Таллинская викторина: занимательные вопросы и задачи для увлеченных химией.
3. Заочный тур. 11 класс. (5)
Распределение баллов по задачам:
| Задача | 1 | 2 | 3 | 4 | 5 |
| Баллы | 3 | 4 | 5 | 6 | 7 |
Смесь метана и этилена со средней молекулярной массой 22 подверглась неполному гидрированию, после чего ее плотность по водороду стала равной 11,25. Какая часть этилена подверглась гидрированию? |
Ответ: гидрированию подверглось 50 % этилена. 1. Рассмотрим состояние газовой смеси до гидрирования. Обозначим объемную долю метана (φ(CH4))
за x, объемную долю этилена (φ(C2H4)) — за y. Тогда, зная относительные
молекулярные массы метана 16x + 28y = 22. Так как в смеси содержатся только метан и этилен, то можно записать следующее уравнение: x + y = 1. Решая систему из уравнений 16x + 28y = 22, x + y = 1, получаем х = 0,5 и y = 0,5. 2. После реакции гидрирования общий объем смеси не изменился:
поэтому объемная доля метана (так как он не участвовал в реакции) осталась той же. Если обозначить объемную долю образовавшегося этана за z, то объемная доля этилена уменьшилась и составила y - z = 0,5 - z. Молекулярная масса смеси после гидрирования составляет Mr(смеси) = DH2(смеси) · Mr(H2) = 11,25 · 2 = 22,5; Mr(С2H6) = 30. Можно записать следующее уравнение для смеси после реакции гидрирования: 16 · 0,5 + 28 · (0,5 - z) + 30 · z = 22,5. Решая это уравнение, получаем, что z = 0,25. Итак, объемная доля этилена до реакции составляла y = 0,5, после реакции —
Очевидно, что доля прореагировавшего этилена составляет z / y = 0,25 / 0,5 = 0,5 или 50% |
18 Декабря 2003 13:09 Раздел каталога :: Ссылка на задачу
|